G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,727
- Solutions
- 3
- Reaction score
- 2,886
- Points
- 113
- Deals
- 1
Úvod
Kyselina lysergová, základný fragment odvodený od námeľových alkaloidov, bola syntetizovaná v štrnástich postupnostiach počnúc 3-beta-karboxyetylindolom. Východiskový materiál bol prevedený na medziprodukt 1-benzoyl-5-keto-1,2,2a-3,4,5-hexahydrobenz-[cd]-indol (3), ktorý obsahuje tri zo štyroch kruhov prítomných v kyseline lysergovej. Tento ketón sa následne transformoval na tetracyklickú zlúčeninu 9-keto-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4.3-fe]-chinolín (8) a odtiaľ na kyselinu lysergovú ( 14). Táto syntéza nie je jednoduchá a vyžaduje si veľa laboratórnych skúseností a chemických znalostí. Okrem toho je tu niekoľko manipulácií s nebezpečnými látkami, ktoré sa musia vykonávať s prísnymi bezpečnostnými opatreniami.
Bod varu: 536,2 ± 50,0 °C pri 760 mm Hg;
Bod topenia: 240 °C;
Molekulová hmotnosť: 268,31 g/mol;
Hustota: 1,4 ± 0,1 g/ml;
Číslo CAS: 82-58-6.
Vybavenie a sklenený riad:
- Oceľový hydrogenačný reaktor 2-3 l;
- Oceľový autokláv 500 ml;
- Laboratórne váhy (vhodné od 0,01 do 500 g);
- banky s okrúhlym dnom 100, 200, 500 ml, 5 a 10 l;
- Vodíkový (H2) kompresor a pôvod;
- Buchnerova banka a lievik (veľký) 5 l [Schottov filter sa môže použiť na malé množstvá];
- Rotovap stroj (veľký);
- Zdroj vákua;
- Separačné lieviky 500 ml a 2 l;
- Dusíkový balón ~ 50 - 70 l (1 bar);
- Uzávery na banky;
- Osolený ľadový vodný kúpeľ;
- 5 L x2, 2 L x2; 1 L x2; 500 ml x2; 100 ml x3; 50 ml x2 Kadičky;
- Sklenená striekačka alebo Pasteurova pipeta;
- Magnetické miešadlo alebo horné miešadlo;
- Vákuová destilačná súprava;
- spätný chladič;
- Retortový stojan a svorka na upevnenie prístroja;
- laboratórny teplomer (-20 °C až 200 °C) s adaptérom na banku;
- Indikačný papier pH;
- sklenená tyčinka a špachtľa;
- 250 W žiarovka.
Reagencie.
- Kyselina 3-indolepropionová (1), 94,6 g (0,5 mol);
- 9,5 l destilovanej vody (H2O);
- ~ 400 g hydroxidu sodného (NaOH);
- 116 g Raneyho niklu (Ni);
- 1050 ml koncentrovanej kyseliny chlorovodíkovej (HCl);
- 2 ml kyseliny sírovej (H2SO4 conc.);
- 210 ml 12N aq roztoku hydroxidu sodného (NaOH);
- 180 ml benzochloridu;
- ~1,5 l metanolu (MeOH);
- ~1,6 l etanolu (EtOH);
- 201,2 ml tionylchloridu (SOCl2);
- 1950 ml disulfidu uhličitého (CS2);
- 240 g chloridu hlinitého (AlCl3);
- 2,5 l benzénu;
- 500 ml 2N hydroxidu sodného (NaOH);
- ~3,2 l dietyléteru (Et2O);
- 3,3 L ľadová kyselina octová (AcOH);
- 352 g (1,1 mol) hydrobromidu pyridínu perbromidu;
- 5 L chloroformu (CHCl3);
- ~1000 g síranu horečnatého (MgSO4);
- 307 g (2,35 mol) metylaminoacetón etylénketal (5);
- 4,5 l benzénu;
- ~500 g Aktívne uhlie (C);
- ~1 l acetónu;
- ~500 g Hydrogenuhličitan sodný (NaHCO3);
- 80 ml Studený anhydrid kyseliny octovej (Ac2O);
- 1,5 g borohydridu sodného (NaBH4);
- 75 ml oxidu siričitého (kvapalina SO2);
- 40 g kyanidu sodného (NaCN prášok);
- 300 ml kyanovodíka (HCN kvapalina);
- 78 ml 1,5 % vodného roztoku hydroxidu draselného (KOH);
- 8,5 g hydratovaného arzeničnanu sodného;
- ~ 50 ml xylénu;
- 100 ml zriedeného roztoku hydroxidu amónneho (NH4OH);
- 16,9 g metoxidu sodného (MeONa).
Postup
1-Benzoyl-3-(beta-karboxyetyl)-2,3-dihydroindol (2)Kyselina 3-indolepropionová (1), 94,6 g (0,5 mol), sa rozpustila v 600 ml vody obsahujúcej 20 g hydroxidu sodného. Roztok sa zmiešal s približne 100 g Raneyho niklového katalyzátora a hydrogenoval sa pri RT v 2-3 l oceľovej hydrogenačnej bombe pri tlaku 3000-4000 psi (207-276 barov) H2. Redukcia sa zvyčajne dokončila za 20 - 30 h, potom sa katalyzátor prefiltroval a premyl malým množstvom vody. Do filtrátu sa pridala koncentrovaná kyselina HCl v množstve 85 ml a roztok sa ochladil. Ak bola redukcia neúplná, v tomto bode sa oddelila nezreagovaná kyselina indolupropiónová a odstránila sa filtráciou. Filtrát sa potom benzoyloval obvyklým Schottenovým-Baumannovým postupom s použitím 210 ml 12N hydroxidu sodného a 180 ml benzoylchloridu. Roztok sa počas celej benzoylácie udržiaval alkalický a teplota sa chladením udržiavala pod 40 °C. Keď benzoylchlorid úplne zreagoval, zmes sa ochladila a okyslila 300 ml koncentrovanej kyseliny HCl. Surový produkt sa prefiltroval a premyl vodou, potom sa extrahoval 4 x 1 l dávkami horúcej vody na odstránenie kyseliny benzoovej. Horúci sirupovitý produkt (2) sa po dekantácii vodného extraktu vykryštalizoval z niekoľkých objemov metanolu; výťažok 103 g (70 %), MP: 151 - 153 °C.
1-Benzoyl-5-keto-1,2,2a,3,4,5-hexahydrobenz-[cd]-indol (3)
1-Benzoyl-3-(beta-karboxyetyl)-2,3-dihydroindol (2), 118 g (0,4 mol), sa zmieša s 200 ml čistého tionylchloridu. Roztok sa nechal stáť 30 min, potom sa 15 - 20 min jemne zahrieval na parnom kúpeli. Prebytočný tionylchlorid sa úplne odparil pod 30 °C vo vákuu a surový chlorid kyseliny sa rozpustil v 200 ml disulfidu uhličitého. Roztok chloridu kyseliny sa potom v tenkom prúde pridal k intenzívne miešanej suspenzii 240 g chloridu hlinitého v 1750 ml disulfidu uhličitého v 5 l banke (v KLADIVE!!!). Komplex sa oddelil a miešanie sa skomplikovalo. Zmes sa zahrievala pod spätným chladením a miešala sa jednu hodinu, aby sa reakcia dokončila, potom sa veľmi opatrne rozložila pridaním 500 g ľadu, 250 ml kyseliny HCl a 500 ml vody. Počas rozkladu sa udržiavalo miešanie a chladenie sa ovplyvňovalo pravidelnou destiláciou disulfidu uhlíka vo vákuu a produkt sa extrahoval 2 l benzénu. Extrakt sa dôkladne premyl 500 ml 2N hydroxidu sodného v troch dávkach a potom vodou. Vysušil sa nad síranom horečnatým a potom sa odparil na malý objem vo vákuu. Pomalé pridávanie niekoľkých objemov éteru spôsobilo kryštalizáciu žltého ketónu (3) . Odfiltroval sa a premyl éterom; výťažok 85,3 g (77 %), MP: 146 - 147 °C. Vzorka bola rekryštalizovaná na analýzu z benzén-éteru.
1-Benzoyl-3-(beta-karboxyetyl)-2,3-dihydroindol (2), 118 g (0,4 mol), sa zmieša s 200 ml čistého tionylchloridu. Roztok sa nechal stáť 30 min, potom sa 15 - 20 min jemne zahrieval na parnom kúpeli. Prebytočný tionylchlorid sa úplne odparil pod 30 °C vo vákuu a surový chlorid kyseliny sa rozpustil v 200 ml disulfidu uhličitého. Roztok chloridu kyseliny sa potom v tenkom prúde pridal k intenzívne miešanej suspenzii 240 g chloridu hlinitého v 1750 ml disulfidu uhličitého v 5 l banke (v KLADIVE!!!). Komplex sa oddelil a miešanie sa skomplikovalo. Zmes sa zahrievala pod spätným chladením a miešala sa jednu hodinu, aby sa reakcia dokončila, potom sa veľmi opatrne rozložila pridaním 500 g ľadu, 250 ml kyseliny HCl a 500 ml vody. Počas rozkladu sa udržiavalo miešanie a chladenie sa ovplyvňovalo pravidelnou destiláciou disulfidu uhlíka vo vákuu a produkt sa extrahoval 2 l benzénu. Extrakt sa dôkladne premyl 500 ml 2N hydroxidu sodného v troch dávkach a potom vodou. Vysušil sa nad síranom horečnatým a potom sa odparil na malý objem vo vákuu. Pomalé pridávanie niekoľkých objemov éteru spôsobilo kryštalizáciu žltého ketónu (3) . Odfiltroval sa a premyl éterom; výťažok 85,3 g (77 %), MP: 146 - 147 °C. Vzorka bola rekryštalizovaná na analýzu z benzén-éteru.
1-Benzoyl-4-bromo-5-keto-1,2,2a,3,4,5-hexahydrobenz-[cd]-indole (4)
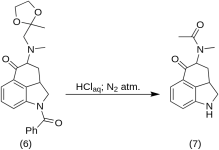
1-Benzoyl-2,2a,3,4-tetrahydro-4-[metyl-(2-metyl-1,2-dioxolan-2-yl-metyl)-amino]-benz-[cd]-indol-5-(1H)-ón (6)
Roztok 270 g (0,76 mol) 1-benzoyl-4-bróm-5-keto-1,2,2a,3,4,5-hexahydrobenz-[cd]-indolu(4) a 307 g (2.35 mol) metylaminoacetón etylén ketalu (5) v 4500 ml suchého benzénu sa refluxovalo pod dusíkom 21 h v 10 L RBF so spätným chladičom. Zmes sa ochladila a 151 g (93,5 %) hydrobromidu metylaminoacetón etylénketalu sa prefiltrovalo, MP: 158 - 159 °C.
Filtrát sa niekoľkokrát premyl ľadovou vodou, potom sa extrahoval 2,5 l studenej zriedenej kyseliny HCl obsahujúcej 150 ml koncentrovanej kyseliny. Kyslé extrakty sa okamžite pridali k prebytku ľadovo studeného zriedeného hydroxidu sodného. Produkt sa extrahoval 1 l chloroformu a chloroformový roztok sa vysušil nad síranom horečnatým, ošetril sa uhlíkom a skoncentroval vo vákuu. Zvyšný ketal-ketón (6 ) sa vykryštalizoval z acetónu; MP: a MP zmesi: 135 - 136 °C, výťažok 220 g (71 %).
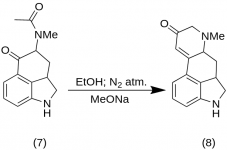
5-Keto-4-[N-metyl-N-acetonylamino]-1,2,2a,3,4,5-hexahydrobenz-[cd]-indol (7)
20 g 1-benzoyl-2,2a,3,4-tetrahydro-4-[metyl-(2-metyl-1,3-dioxolan-2-yl-metyl)-amino]-benz-[cd]-indol-5-(1H)-ón (6 ) sa rozpustil v zmesi 250 ml koncentrovanej kyseliny HCl a 250 ml vody a roztok sa uchovával pod dusíkom pri 37 °C v 3-5 l RBF počas piatich dní. Zmes sa ochladila, ošetrila uhlíkom, prefiltrovala a filtrát sa zahustil vo vákuu na malý objem. Zvyšok sa spracoval s prebytkom hydrogenuhličitanu sodného; produkt sa extrahoval studeným chloroformom a rozpúšťadlo sa odstránilo vo vákuu pri RT. Surový diketón (7 ) sa rozomlel na prášok, rozmiešal s približne 75 ml benzén-éteru v pomere 1:1 a prefiltroval; výťažok 9,8 g (77 %), MP: 105 - 107 °C. Vzorka na analýzu sa rekryštalizovala z benzén-éteru alebo etanolu; MP: 109 - 110 °C; monohydrochlorid sa získal zo zriedeného etanolu; MP: 200 °C dec.
9-Keto-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín (8)
25 g 5-Keto-4-[N-metyl-N-acetonyl]-amino-1,2,2a,3,4,5-hexahydrobenz-[cd]-indolu (7 ) sa zmieša s 550 ml absolútneho etanolu. Zmes sa miešala pod dusíkom a ochladila na -15 °C v 2-5 l RBF. Potom sa pridal metoxid sodný, 16,9 g, a zmes sa desať minút miešala pri teplote -10 °C až -12 °C. Reakčná zmes sa ochladila na -25 °C a produkt sa prefiltroval na 6,5-palcovom Buchnerovom lieviku a premyl sa trochou studeného etanolu a éteru. Pri minimálnej expozícii vzduchu (obsahuje metoxid sodný!) sa surový ketón (8) okamžite rozmiešal s trochou ľadovej vody a znovu sa prefiltroval. Premyl sa ľadovou vodou, etanolom a éterom; výťažok 16,2 g (69 %), MP: 145 - 147 °C. Analytická vzorka sa rekryštalizovala zo zriedeného etanolu; MP: 155 - 157 °C; pripravil sa dihydrochlorid a rekryštalizoval sa z vodného acetónu; MP: 270 °C dec.
4-acetyl-9-keto-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín (9)
9-keto-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín (8), 24 g, sa pridal k 80 ml studeného anhydridu kyseliny octovej. Zmes sa udržiavala pri teplote 25 °C v 200 ml RBF približne 5 min, potom sa dôkladne ochladila a produkt (9 ) sa prefiltroval a premyl éterom; výťažok 20,5 g (76 %), mp: 167-170 °C. Druhá plodina sa získala odparením filtrátu; tým sa zvýšil celkový výťažok na 82 %. Vzorka sa rekryštalizovala z acetón-etanolu; MP: 169-170 °C; Hydrochlorid sa pripravil v etanole a rekryštalizoval sa z vodného etanolu; MP: 250 °C dec.
9-keto-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín (8), 24 g, sa pridal k 80 ml studeného anhydridu kyseliny octovej. Zmes sa udržiavala pri teplote 25 °C v 200 ml RBF približne 5 min, potom sa dôkladne ochladila a produkt (9 ) sa prefiltroval a premyl éterom; výťažok 20,5 g (76 %), mp: 167-170 °C. Druhá plodina sa získala odparením filtrátu; tým sa zvýšil celkový výťažok na 82 %. Vzorka sa rekryštalizovala z acetón-etanolu; MP: 169-170 °C; Hydrochlorid sa pripravil v etanole a rekryštalizoval sa z vodného etanolu; MP: 250 °C dec.
4-Acetyl-9-hydroxy-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín (10)
10 g 4-acetyl-9-keto-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroxindolo-[4,3-fg]-chinolínu (9 ) sa pridalo do zmesi 150 ml metanolu a 10 ml vody v 500 ml RBF. Pridal sa 1,5 g borohydridu sodného a reakcia sa nechala prebiehať pri RT do malého objemu a pridala sa zmes 15 ml konk. kyseliny HCl a 60 ml vody. Chlorovodík (10) , ktorý sa oddelil pri chladení, sa prefiltroval a premyl metanolom, 9,0 g (79 %). Vzorka sa rekryštalizovala zo zriedeného etanolu; MP: 245-246 °C dec.
4-acetyl-9-chlór-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín hydrochlorid (11)
4-acetyl-9-hydroxy-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín hydrochlorid (10), 3.1 g sa rozpustil v 75 ml kvapalného oxidu siričitého v sklenenej vložke v 500 ml oceľovom autokláve. Pridalo sa 1,2 ml tionylchloridu, nádoba sa uzavrela a udržiavala pri teplote 25 °C počas 6 h. Autokláv sa odvzdušnil a reakčná zmes sa odstránila. Oxid siričitý sa nechal odparovať, pričom objem roztoku sa udržiaval konštantný pomalým pridávaním suchého éteru. Amorfný chlórhydrochlorid (11 ) sa prefiltroval, premyl éterom a vysušil vo vákuu, MP: 130 - 135 °C dec. Výťažok 3,5 g. Použitím 9-beta-epimérového alkoholu v tejto reakcii sa získal rovnaký chlorid v porovnateľnom výťažku.
4-acetyl-9-kyano-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín (12)
Suchý, práškový kyanid sodný, 40 g, sa pridal k 300 ml ľadového kvapalného kyanovodíka. Zmes sa premiešala a ochladila v ľade a pridalo sa 7,5 g surového amorfného 4-acetyl-9-chlór-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo[4,3f/g]-chinolín hydrochloridu ( 11 ). Miešanie pokračovalo v 500 ml RBF počas 30 min, potom sa kyanovodík rýchlo vydestiloval za zníženého tlaku pri teplote približne 10 °C. Zvyšok sa zmiešal s chloroformom a ľadovou vodou a vzniknutá zmes sa prefiltrovala. Organická vrstva sa oddelila a vodná fáza sa dvakrát extrahovala chloroformom. Spojené extrakty sa vysušili nad síranom horečnatým, odfarbili a rozpúšťadlo sa vydestilovalo vo vákuu. Produkt (12) sa vykryštalizoval z etylacetátu; výťažok 3,3 g (54 % z celkového množstva na báze alkoholhydrochloridu), m.p. 172 - 174 °C. Rekryštalizáciou z toho istého rozpúšťadla sa m.p. zvýšil na 181-182 °C.
Suchý, práškový kyanid sodný, 40 g, sa pridal k 300 ml ľadového kvapalného kyanovodíka. Zmes sa premiešala a ochladila v ľade a pridalo sa 7,5 g surového amorfného 4-acetyl-9-chlór-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo[4,3f/g]-chinolín hydrochloridu ( 11 ). Miešanie pokračovalo v 500 ml RBF počas 30 min, potom sa kyanovodík rýchlo vydestiloval za zníženého tlaku pri teplote približne 10 °C. Zvyšok sa zmiešal s chloroformom a ľadovou vodou a vzniknutá zmes sa prefiltrovala. Organická vrstva sa oddelila a vodná fáza sa dvakrát extrahovala chloroformom. Spojené extrakty sa vysušili nad síranom horečnatým, odfarbili a rozpúšťadlo sa vydestilovalo vo vákuu. Produkt (12) sa vykryštalizoval z etylacetátu; výťažok 3,3 g (54 % z celkového množstva na báze alkoholhydrochloridu), m.p. 172 - 174 °C. Rekryštalizáciou z toho istého rozpúšťadla sa m.p. zvýšil na 181-182 °C.
9-karbometoxy-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolín (13)
Práve uvedený produkt (12 ), 1,0 g, sa zmieša s 15 ml metanolu a 0,25 ml vody. Zmes sa ochladila a pomaly sa pridali 2 ml koncentrovanej kyseliny sírovej. Roztok bol uzavretý v sklenenej skúmavke pod dusíkom a zahrievaný pri 100 °C počas 23 až 24 h v 100 mL RBF so spätným chladičom. Zmes sa upravila dekolorizovaným uhlím a potom sa skoncentrovala vo vákuu na približne 10 ml. Naliala sa na zmes chloroformu (30 ml), ľadu a 10 g hydrogenuhličitanu sodného. Chloroformová vrstva sa oddelila a vodná fáza sa extrahovala 3 x 10 ml dávkami chloroformu. Spojené extrakty sa vysušili nad síranom horečnatým, odparili do sucha a produkt (13) sa vykryštalizoval z benzénu; výťažok 0,51 g (53 %), MP: 159 - 160 °C. Rekryštalizoval sa z etylacetátu; MP: 160 - 161 °C.
Práve uvedený produkt (12 ), 1,0 g, sa zmieša s 15 ml metanolu a 0,25 ml vody. Zmes sa ochladila a pomaly sa pridali 2 ml koncentrovanej kyseliny sírovej. Roztok bol uzavretý v sklenenej skúmavke pod dusíkom a zahrievaný pri 100 °C počas 23 až 24 h v 100 mL RBF so spätným chladičom. Zmes sa upravila dekolorizovaným uhlím a potom sa skoncentrovala vo vákuu na približne 10 ml. Naliala sa na zmes chloroformu (30 ml), ľadu a 10 g hydrogenuhličitanu sodného. Chloroformová vrstva sa oddelila a vodná fáza sa extrahovala 3 x 10 ml dávkami chloroformu. Spojené extrakty sa vysušili nad síranom horečnatým, odparili do sucha a produkt (13) sa vykryštalizoval z benzénu; výťažok 0,51 g (53 %), MP: 159 - 160 °C. Rekryštalizoval sa z etylacetátu; MP: 160 - 161 °C.
Syntetická kyselina dl-Lysergová (14)
Zmes 9-karbometoxy-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolínu (13), 3,9 g, a 78 ml 1,5 % roztoku hydroxidu draselného sa refluxovala 30 min pod dusíkom. Pridal sa hydratovaný arzeničnan sodný, 8,5 g, a Raneyho nikel (16 g, mokrý), predtým deaktivovaný varením v xylénovej suspenzii, a zmes sa zahrievala pod spätným chladením a miešala v dusíkovej atmosfére 20 hodín v 200 ml RBF so spätným chladičom. Roztok sa upravil uhlíkom a surová kyselina lysergová (14 ) sa vyzrážala neutralizáciou na pH 5,6. Filtrovala sa a premyla vodou; výťažok 1,04 g, MP: 240-242 °C dec. Získala sa aj druhá plodina, 0,16 g, MP: 233-235 °C dec.; celkový výťažok 30 %. Kyselinu bolo možné prečistiť rozpustením v zriedenom hydroxide amónnom, ošetrením odfarbovacím uhlím a opätovným vyzrážaním oxidom uhličitým, MP: 242-243 °C dec; zmes s kyselinou dl-lyzergovou vyrobenou z prírodnej kyseliny d-lyzergovej mala tiež 242-243 °C dec. Bezvodá kyselina sa získala niekoľkohodinovým sušením vo vákuu pri 150 °C.
Zmes 9-karbometoxy-7-metyl-4,5,5a,6,6a,7,8,9-oktahydroindolo-[4,3-fg]-chinolínu (13), 3,9 g, a 78 ml 1,5 % roztoku hydroxidu draselného sa refluxovala 30 min pod dusíkom. Pridal sa hydratovaný arzeničnan sodný, 8,5 g, a Raneyho nikel (16 g, mokrý), predtým deaktivovaný varením v xylénovej suspenzii, a zmes sa zahrievala pod spätným chladením a miešala v dusíkovej atmosfére 20 hodín v 200 ml RBF so spätným chladičom. Roztok sa upravil uhlíkom a surová kyselina lysergová (14 ) sa vyzrážala neutralizáciou na pH 5,6. Filtrovala sa a premyla vodou; výťažok 1,04 g, MP: 240-242 °C dec. Získala sa aj druhá plodina, 0,16 g, MP: 233-235 °C dec.; celkový výťažok 30 %. Kyselinu bolo možné prečistiť rozpustením v zriedenom hydroxide amónnom, ošetrením odfarbovacím uhlím a opätovným vyzrážaním oxidom uhličitým, MP: 242-243 °C dec; zmes s kyselinou dl-lyzergovou vyrobenou z prírodnej kyseliny d-lyzergovej mala tiež 242-243 °C dec. Bezvodá kyselina sa získala niekoľkohodinovým sušením vo vákuu pri 150 °C.
Attachments
Last edited: