- Language
- 🇺🇸
- Joined
- Oct 17, 2023
- Messages
- 86
- Reaction score
- 101
- Points
- 33
- Deals
- 22
SÍNTESE:
Uma solução de 100 g de 2,5-dimetoxibenzaldeído em 220 g de nitrometano foi tratada com 10 g de acetato de amónio anidro e aquecida num banho de vapor durante 2,5 h com agitação ocasional. A mistura reacional, de cor vermelha intensa, foi removida do excesso de nitrometano sob vácuo e o resíduo cristalizou espontaneamente. Este nitroestireno bruto foi purificado por trituração sob IPA, filtragem e secagem ao ar, para obter 85 g de 2,5-dimetoxi-beta-nitroestireno como um produto amarelo-alaranjado de pureza adequada para a etapa seguinte. Pode obter-se uma purificação adicional por recristalização a partir de IPA em ebulição.
Num balão de fundo redondo de 2 L equipado com um agitador magnético e colocado sob uma atmosfera inerte, foram adicionados 750 mL de THF anidro, contendo 30 g de LAH. Em seguida, adicionou-se, em solução de THF, 60 g de 2,5-dimetoxi-beta-nitrostyrene. A solução final era de cor amarelo-castanho sujo e foi mantida à temperatura de refluxo durante 24 h. Após arrefecimento, o excesso de hidreto foi destruído pela adição gota a gota de IPA. Em seguida, foram adicionados 30 mL de NaOH a 15% para converter os sólidos inorgânicos numa massa filtrável. A mistura reacional foi filtrada e o bolo filtrante foi lavado primeiro com THF e depois com MeOH. Os licores-mãe e as lavagens combinados
foram libertados do solvente sob vácuo e o resíduo foi suspenso em 1,5 L de H2O. Este foi acidificado com HCl, lavado com 3x100 mL de CH2Cl2, tornado fortemente básico com NaOH a 25% e reextraído com 4x100 mL de CH2Cl2. Os extractos combinados foram removidos do solvente sob vácuo, dando origem a 26 g de resíduo oleoso, que foi destilado a 120-130 °C a 0,5 mm/Hg para dar 21 g de um óleo branco, 2,5-dimetoxi-fenetilamina (2C-H), que apanha rapidamente dióxido de carbono do ar.
A uma solução bem agitada de 24,8 g de 2,5-dimetoxifenetilamina em 40 mL de ácido acético glacial, foram adicionados 22 g de bromo elementar dissolvido em 40 mL de ácido acético. Após alguns minutos, verificou-se a formação de sólidos e a evolução simultânea de calor considerável. A mistura reacional foi deixada voltar à temperatura ambiente, filtrada e os sólidos foram lavados com moderação com ácido acético frio. Este era o sal de bromidrato. Existem muitas formas complicadas de sal, tanto polimorfos como hidratos, que podem tornar o isolamento e a caraterização do 2C-B traiçoeiros. O caminho mais feliz é formar o sal cloridrato insolúvel por meio da base livre. Toda a massa de sal molhado em ácido acético foi dissolvida em H2O quente, tornada básica a pelo menos pH 11 com NaOH a 25% e extraída com 3x100 mL de CH2Cl2. A remoção do solvente deu 33,7 g de resíduo que foi destilado a 115-130 °C a 0,4 mm/Hg.
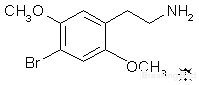
O óleo branco, 27,6 g, foi dissolvido em 50 mL de H2O contendo 7,0 g de ácido acético. Esta solução clara foi agitada vigorosamente e tratada com 20 mL de HCl concentrado. Verificou-se a formação imediata do sal anidro do cloridrato de 2,5-dimetoxi-4-bromofenetilamina (2C-B). Esta massa de cristais foi removida por filtração (pode ser solta consideravelmente pela adição de mais 60 mL de H2O), lavada com um pouco de H2O, e depois com várias porções de 50 mL de Et2O. Quando completamente seco ao ar, foram obtidos 31,05 g de agulhas brancas finas, com um mp de 237-239 °C com decomposição. Quando há demasiado H2O presente no momento da adição do HCl concentrado final, obtém-se uma forma hidratada de 2C-B. O sal de bromidrato funde a 214,5- 215 °C. O sal de acetato tem uma temperatura de fusão de 208-209 °C.
DOSAGEM: 12 - 24 mg.
DURAÇÃO: 4 - 8 h.
>> Se alguém tentar fazer esta síntese e puder apresentar fotografias e mais pormenores, seria bom, ou mesmo um vídeo, se não for pedir muito, penso que muitos estariam interessados.
Uma solução de 100 g de 2,5-dimetoxibenzaldeído em 220 g de nitrometano foi tratada com 10 g de acetato de amónio anidro e aquecida num banho de vapor durante 2,5 h com agitação ocasional. A mistura reacional, de cor vermelha intensa, foi removida do excesso de nitrometano sob vácuo e o resíduo cristalizou espontaneamente. Este nitroestireno bruto foi purificado por trituração sob IPA, filtragem e secagem ao ar, para obter 85 g de 2,5-dimetoxi-beta-nitroestireno como um produto amarelo-alaranjado de pureza adequada para a etapa seguinte. Pode obter-se uma purificação adicional por recristalização a partir de IPA em ebulição.
Num balão de fundo redondo de 2 L equipado com um agitador magnético e colocado sob uma atmosfera inerte, foram adicionados 750 mL de THF anidro, contendo 30 g de LAH. Em seguida, adicionou-se, em solução de THF, 60 g de 2,5-dimetoxi-beta-nitrostyrene. A solução final era de cor amarelo-castanho sujo e foi mantida à temperatura de refluxo durante 24 h. Após arrefecimento, o excesso de hidreto foi destruído pela adição gota a gota de IPA. Em seguida, foram adicionados 30 mL de NaOH a 15% para converter os sólidos inorgânicos numa massa filtrável. A mistura reacional foi filtrada e o bolo filtrante foi lavado primeiro com THF e depois com MeOH. Os licores-mãe e as lavagens combinados
foram libertados do solvente sob vácuo e o resíduo foi suspenso em 1,5 L de H2O. Este foi acidificado com HCl, lavado com 3x100 mL de CH2Cl2, tornado fortemente básico com NaOH a 25% e reextraído com 4x100 mL de CH2Cl2. Os extractos combinados foram removidos do solvente sob vácuo, dando origem a 26 g de resíduo oleoso, que foi destilado a 120-130 °C a 0,5 mm/Hg para dar 21 g de um óleo branco, 2,5-dimetoxi-fenetilamina (2C-H), que apanha rapidamente dióxido de carbono do ar.
A uma solução bem agitada de 24,8 g de 2,5-dimetoxifenetilamina em 40 mL de ácido acético glacial, foram adicionados 22 g de bromo elementar dissolvido em 40 mL de ácido acético. Após alguns minutos, verificou-se a formação de sólidos e a evolução simultânea de calor considerável. A mistura reacional foi deixada voltar à temperatura ambiente, filtrada e os sólidos foram lavados com moderação com ácido acético frio. Este era o sal de bromidrato. Existem muitas formas complicadas de sal, tanto polimorfos como hidratos, que podem tornar o isolamento e a caraterização do 2C-B traiçoeiros. O caminho mais feliz é formar o sal cloridrato insolúvel por meio da base livre. Toda a massa de sal molhado em ácido acético foi dissolvida em H2O quente, tornada básica a pelo menos pH 11 com NaOH a 25% e extraída com 3x100 mL de CH2Cl2. A remoção do solvente deu 33,7 g de resíduo que foi destilado a 115-130 °C a 0,4 mm/Hg.
O óleo branco, 27,6 g, foi dissolvido em 50 mL de H2O contendo 7,0 g de ácido acético. Esta solução clara foi agitada vigorosamente e tratada com 20 mL de HCl concentrado. Verificou-se a formação imediata do sal anidro do cloridrato de 2,5-dimetoxi-4-bromofenetilamina (2C-B). Esta massa de cristais foi removida por filtração (pode ser solta consideravelmente pela adição de mais 60 mL de H2O), lavada com um pouco de H2O, e depois com várias porções de 50 mL de Et2O. Quando completamente seco ao ar, foram obtidos 31,05 g de agulhas brancas finas, com um mp de 237-239 °C com decomposição. Quando há demasiado H2O presente no momento da adição do HCl concentrado final, obtém-se uma forma hidratada de 2C-B. O sal de bromidrato funde a 214,5- 215 °C. O sal de acetato tem uma temperatura de fusão de 208-209 °C.
DOSAGEM: 12 - 24 mg.
DURAÇÃO: 4 - 8 h.
>> Se alguém tentar fazer esta síntese e puder apresentar fotografias e mais pormenores, seria bom, ou mesmo um vídeo, se não for pedir muito, penso que muitos estariam interessados.