Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 264
- Reaction score
- 292
- Points
- 63
Dextroamfetamin (D-AMP) tilhører en klasse af stimulanser til centralnervesystemet. Food and Drug Administration i USA klassificerer det som et stof på liste II med et stort potentiale for misbrug. Medicin med øjeblikkelig og forsinket frigivelse af amfetamin er godkendt af FDA til behandling af ADHD og narkolepsi hos både voksne og børn. Dextroamfetamin adskiller sig fra sit spejlbillede - levoamfetamin - fordi det har en mere udtalt stimulering af nervesystemet på grund af dopamin og mindre - på grund af noradrenalin.
Syntese af dextroamfetamin fra P2P
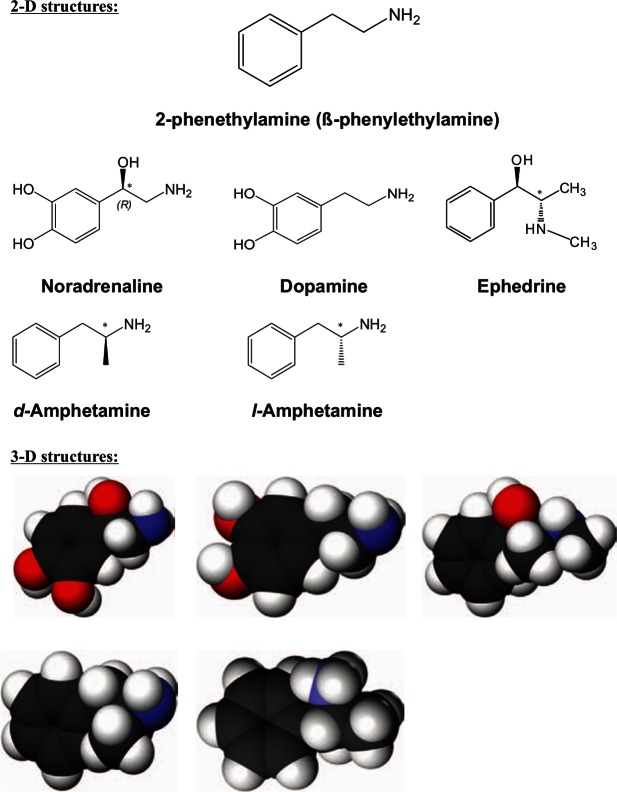
Fysisk-kemiske egenskaber og former for stoffet.
Grundlæggende har dextroamfetamin såvel som amfetaminracemat udseendet af en farveløs flygtig olieagtig væske med en karakteristisk "fiskeagtig" lugt og er godt opløselig i organiske opløsningsmidler. Dens kogepunkt er 200-203 °C. Enantiomeren kan have et pulveragtigt udseende med dannelse af små "sten" i hvid eller lysegul/cremefarve, med en svag lugt, svagt hygroskopisk, delvist opløselig i vand, når den er i form af en tablet. Det findes oftest i form af sulfat, hydrochlorid, sucrat og meget sjældent i form af fosfat. Som regel er dextroamfetamin en del af forskellige lægemidler som "Aderral" og "Dexedrine", hvor det findes i form af sukrat og sulfat i koncentrationer på 25% af det samlede volumen. Det er også en del af "Vyvanse", "Elvanse", "Tyvense", hvor det er i den proaktive tilstand af dimesylat lysdexamfetamin; fermentering med l-lysin metaboliserer det til den aktive form af d-amfetamin; "Dexedrine". Andre handelsnavne på lægemidler omfatter: Dexedrinsulfat, Afatin, d-Amfetasul, Domafate Obesedrin, Dexten, Maxiton, Sympamin, Simpamina-D, Albemap, Dadex, Ardex, Dexalone, Amsustain, Betafedrina, d-Betaphedrin, Diocurb, Dextrostat.
Farmakokinetik.
Når det indgives, metaboliseres amfetamin ved hydroxylering, hvor det vigtigste cytokrom er CYP2D6, beta-hydroxylering (DBH) og oxidativ deaminering (FMO3); der er andre enzymer, der er mindre involveret i metaboliseringen af amfetamin, såsom butyrat-CoA-ligase og glycin-N-acyltransferase. Biotilgængeligheden (med uændret gastrointestinal pH) når 70-75% for racemat og op til 80-83% for dextroamfetamin. Bindingen med plasmaproteiner når 15-30% ifølge forskellige kilder hos raske mennesker, distributionsvolumenet er moderat, stoffet passerer aktivt gennem blod-hjerne-barrieren med en variabel koefficient på 17p. T1/2 er ca. 7-15 timer, afhængigt af mange faktorer, herunder urinens pH (med en acceleration af halveringstiden ved lavere værdier). Imax - 15-70 minutter. Dødelig dosis af d-isomer af amfetamin er ikke blevet undersøgt; der er dog teoretiske konklusioner om store værdier af LD 50 på 5-10% fra de tilgængelige ekstrapolerede data for standardracematet af amfetaminsulfat (98-130 mg/kg). Amfetamin elimineres i næsten de samme kvalitative indikatorer for kendte metabolitter, men mængden af hippursyre, benzoylglycuronid og norephedrin er betydeligt mindre (60 % af de samlede data), hvilket skyldes dette racemats specificitet i forbindelse med metabolisme på deamineringsniveau. I undersøgelser af gnavere blev der påvist et markant fald i genotoksicitet i modsætning til standardamfetaminracematet i en dosis på 4600 mg/ml.
Virkningsmekanisme.
Den farmakodynamiske virkningsmekanisme adskiller sig næsten ikke fra den grundlæggende form af amfetamin. Gennem hæmning og reversering af serotonin-, noradrenalin- og dopamintransportører, interaktion med TAAR1, hvilket i sidste ende fører til en stigning i koncentrationen af monoaminer og katekolaminer samtidigt i den synaptiske kløft (kløften er 10-50 nm bred mellem membranerne, kanterne styrkes af intercellulære kontakter). Et vigtigt træk ved dextroamfetamin specifikt er det faktum, at affiniteten for den højresidede enantiomer med TAAR1 er meget større (med 15-30% ifølge forskellige kilder), og VMAT2 fanger en mindre mængde af denne enantiomer, og den mindste affinitet for serotonintransportøren i modsætning til den venstresidede, og belastningen af sådanne systemer som CDK5R1, DLG1 og CAMKIIAA er betydeligt mindre med tilsvarende kliniske virkninger.
Ikke mindre vigtigt er det videnskabelige faktum identificeret af Novascreen BioSciences Corporation, at på grund af lavere affinitet for en række receptorer (a1, a2, b-adrenoreceptorer, mu-opioid, histamin, CCK, NK, GABA, ETeA og andre) er sværhedsgraden af både uønskede kliniske bivirkninger og andre negative konsekvenser på molekylært niveau betydeligt lavere, hvilket bestemmer prioriteringen af denne særlige form for stoffet med bevarelse af de tilsvarende ønskede kliniske virkninger. Nettoeffekten af disse multiple virkningsegenskaber er, at d-amfetamin øger "tilgængeligheden" eller koncentrationsevnen af katekolaminer i det ekstracellulære rum ved at vende transporten af katekolaminer fra den terminale ende af neuronet, hvilket også er et af kendetegnene ved den højredrejende enantiomer. Indikatorerne for hæmning af optagelsen af [3 H] i rottehjernens synaptosomer af d-enantiomeren varierer og adskiller sig markant fra amfetaminracemat. For noradrenalin er Ki = nM ved en værdi på 45-50, for dopamin 82-200, for 5-HT varierer indikatorerne fra 1840 til 3830 i rottehjernemodeller. En mere "blød" effekt af afhængighedscyklussen fra denne form for amfetamin er en konsekvens af en relativt lavere overekspression af FosB i nucleus accumbens, tilstedeværelsen af positive effekter og fraværet af inhibering af CREB af protein- og serinfosfotaser netop på grund af lavere affinitet og indflydelse på de glutamaterge og serotoninerge systemer. Neurokemiske virkninger har til sammenligning også en særlig evne; i Heal- og Wickens-undersøgelserne blev der påvist ændringer i motorisk aktivitet, hvor dens maksimale værdi var 3-4 gange mindre end ved indtagelse af amfetaminhydrochlorid eller sulfat, hvilket er direkte relateret til hastigheden og den molekylære korrektion af dopaminudstrømningen i hjernens striatum.
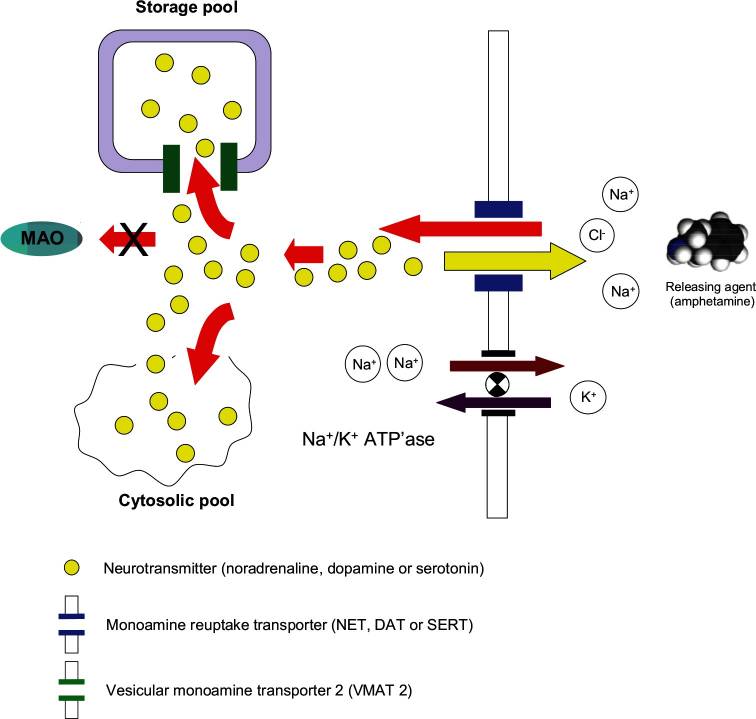
Selvom in vitro-eksperimenter giver et godt indblik i individuelle mekanismer, kan effekten af amfetamin i forhold til andre indirekte monoaminagonister, for eksempel klassiske genoptagelseshæmmere, kun estimeres ud fra in vivo-eksperimenter. Vi har brugt intracerebral mikrodialyse med to sonder til at undersøge in vivo-effekterne af d- og l-amfetamin i den spontant hypertensive rotte (SHR), som er blevet foreslået som en gnavermodel for ADHD. Begge isomerer af amfetamin øgede dosisafhængigt de ekstracellulære koncentrationer af noradrenalin i den præfrontale cortex (PFC) og dopamin i striatum. Farmakodynamikken i deres virkninger er typisk for dem, der er rapporteret for monoaminfrigørende midler, dvs. en hurtig virkning med maksimale stigninger i noradrenalin- og dopaminudstrømning, der forekommer efter 30-45 minutter, store virkninger (400-450 % af baseline for noradrenalin og 700-1500 % af baseline for dopamin) med et relativt hurtigt fald efter maksimum. Selvom der ikke er medtaget nogen sammenlignende resultater i denne gennemgang, er omfanget af de stigninger, der produceres af amfetamins isomerer, større end dem, der er rapporteret for klassiske genoptagelseshæmmere som atomoxetin eller bupropion, og der er ikke noget dosis-effekt-loft for amfetamins handlinger.
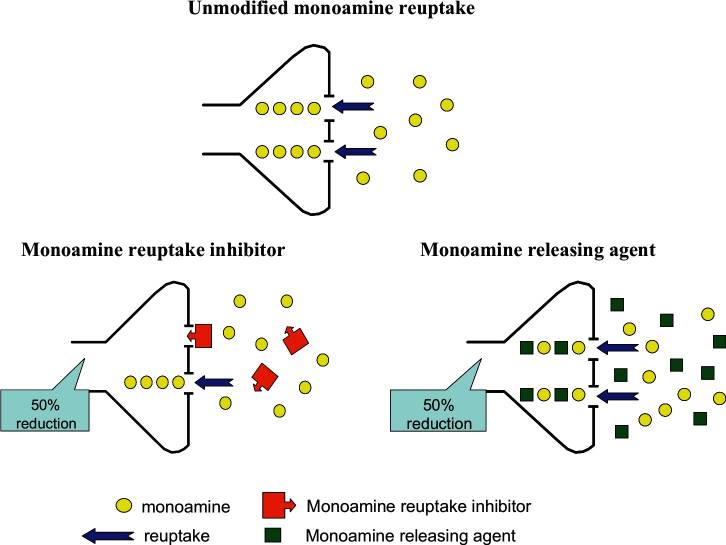
Når man sammenligner stoffernes virkning på udstrømningen af katekolaminer i PFC, er det vigtigt at tage højde for den meget usædvanlige neuroanatomi i dette hjerneområde. Tætheden af DAT-steder på dopaminerge neuroner i PFC er meget lav, og som følge heraf bliver det meste dopamin, der frigives, bundet via NET i noradrenerge neuroner. Selv om der er få DAT-steder på dopaminerge neuroner i PFC, er deres genoptagelseskapacitet tilstrækkelig til, at amfetamin kan fremkalde en betydelig dopaminfrigivelse fra dem, selv om det er blevet foreslået, at en stor del af dopaminfrigivelsen i PFC kommer fra noradrenerge neuroner. I Shires udviklingsstudier på in vivo-modeller blev der påvist en statistisk signifikant forskel. D-AMP påvirkede de kognitive komponenter i impulskontrol forskelligt: andelen af impulsive valg faldt med samme niveau af belønning, hvilket også bekræfter effektiviteten af denne enantiomer.
Anvendelsesmetoder og doser.
Rekreativ dosering af amfetamin d-enantiomer starter fra 40-60 mg ved oral brug, i tilfælde af nuværende tolerance kan startdosis øges op til 120-160 mg ved en enkelt oral brug. Ved intranasal administration anbefales det at bruge en startdosis på 30-50 mg. Parenteral administration af denne form er kun tilladt i tilfælde af, at der opnås en ren opløsning. Eventuelle tabletter eller pulvere anbefales kun til brug ved oral og intranasal administration. Ved parenteral indgivelse er startdosis 0,15-0,24 mg/kg.
Klinisk præsentation af amfetaminforgiftning.
Symptomerne ovenfor er "milde", deres sværhedsgrad er op til 40% mindre end for den kombinerede form. Derfor forekommer sådanne negative uønskede virkninger som vandladningsbesvær, hjerterytmeforstyrrelser, øget hjertefrekvens, øget blodtryk, øget svedtendens, høj kropstemperatur, kvalme, pupiludvidelse udelukkende ved høje doser og er proportionalt forskellige i sammenligning med racemat.
1. Eufori og en følelse af øget energi;
2. Langvarig vågenhed;
3. Grandiose ideer eller handlinger;
4. Voldelig eller aggressiv adfærd;
5. Bekræftelsesbias;
6. Labilitet i humøret;
7. Adfærd præget af gentagne stereotyper;
8. Auditive, visuelle eller taktile illusioner;
9. Forvrængning af personlighed;
10. Undertrykkelse af appetitten.
Personer, der bruger D-AMP, skal også have mindst to af følgende tegn for at blive diagnosticeret:
1. Takykardi;
2. Arteriel hypertension;
3. Sved og feberagtige kulderystelser;
4. Kvalme eller opkastning;
5. Muskelsvaghed;
6. Smerter eller ubehag bag brystbenet;
7. Psykomotorisk uro;
8. Udvidelse af pupiller.
Symptomer på D-AMP-forgiftning omfatter hovedsageligt tegn på komplikationer i hjerte-kar-systemet og nervesystemet. Åndedrætsforstyrrelser udvikles sjældnere.
Hjerteforstyrrelser: hypertension og takykardi er de mest almindelige, når man tager lave doser. Indledende bradykardi er også mulig på grund af en stigning i den parasympatiske tone. Arytmier (supraventrikulære er hyppige) kan være forårsaget af en sympatisk krise eller en blokade af hurtige natriumkanaler. Iskæmi og myokardieinfarkt forårsages af koronar spasme, som når et maksimum 30 minutter efter intranasal D-AMP-brug og falder sammen med den højeste koncentration af stoffet i blodet. Yderligere koronarspasmer kan udvikles efter 90 minutter, hvilket er forbundet med ophobning af D-AMP-metabolitter. En stigning i blodpladeaggregering fører til dannelse af blodpropper i koronarkarrene. Desuden øges myokardiets iltbehov. En sjælden komplikation er aortaruptur.
Særlige instruktioner, interaktioner med andre stoffer.
De absolutte kontraindikationer for brugen af enhver form for amfetamin er: alvorlig vaskulær aterosklerose, enhver symptomatisk kardiovaskulær sygdom, MAO-indtagelse (og 14 dage efter den sidste brug af stoffet i denne gruppe), glaukom, hyperthyreoidisme.
"Ikke-ADIOS"-reglen:
Non-Alcohol - det anbefales ikke at bruge sammen med alkohol.
Non-Dissociatives - det anbefales ikke at bruge sammen med dissociative stoffer.
Non-iMAO - det anbefales ikke at bruge det sammen med monoaminoxidasehæmmere.
Non-Opiates - det anbefales ikke at bruge sammen med opioidreceptoragonister.
Ikke-stimulatorer - det anbefales ikke at bruge sammen med stimulanser.
1. Når man bruger D-AMP sammen med lægemidler fra gruppen af PDE-5-hæmmere, øges risikoen for at udvikle bivirkninger af begge stoffer. Mest almindelige bivirkninger: svær hovedpine af spastisk karakter, kvalme. Forekomsten af alvorlige kritiske tilstande er lav.
2. Ved brug af D-AMP sammen med marihuana er der risiko for forekomst af forhøjet blodtryk, hovedpine, fin tremor, tørhed i munden. Sandsynligheden for at udvikle alvorlige kritiske tilstande er lav.
3. Ved brug af D-AMP sammen med neuroleptika/tranquilizers er der stor risiko for at udjævne D-AMP's hovedvirkninger. Sandsynligheden for at udvikle alvorlige kritiske tilstande er lav (i tilfælde, hvor der ikke er kontraindikationer for at tage neuroleptika).
4. Det anbefales ikke at bruge D-AMP under behandling med antibakterielle, antivirale og svampedræbende lægemidler, hormoner og antikoagulantia.
5. Det anbefales ikke at bruge D-AMP under kirurgiske indgreb og i tiden før og efter det i en bestemt periode (perioden identificeres individuelt).
6. Det anbefales ikke at bruge D-AMP, hvis der er diagnosticeret en lidelse i det kardiovaskulære system, nyrerne, leveren, lungerne eller centralnervesystemet.
7. Det anbefales ikke at bruge D-AMP under graviditet og amning.
I to tidligere offentliggjorte undersøgelser sammenlignede Jasinski og Krishnan de subjektive virkninger af IR d-amfetamin hos stoferfarne frivillige mennesker, når disse forbindelser blev administreret intravenøst og oralt. I forsøget, hvor de sammenlignede disse stoffer efter oral administration, fremkaldte IR d-amfetamin (40 mg (29,6 mg d-amfetaminbase)) en statistisk signifikant stigning i forhold til placebo i "Drug liking" på Drug Rating Questionnaire - Subject (DQRS)-skalaen, hvorimod den tilsvarende dosis d-amfetamin (100 mg, oral) ikke gjorde det. Desuden var tidspunktet for den maksimale farmakologiske virkning af d-amfetamin væsentligt forsinket sammenlignet med IR d-amfetamin, nemlig 3,0 timer mod 1,5-2,0 timer. Når d-amfetamin blev givet i en øget dosis på 150 mg, øgede det signifikant DQRS-scoren for "Drug liking" i samme omfang som IR d-amfetamin (40 mg oralt). Imidlertid var den maksimale effekt af den højere dosis d-amfetamin endnu mere forsinket, ved 4.0 h. Når den intravenøse rute blev udforsket, producerede IR d-amfetamin (20 mg intravenøs) en maksimal 'Drug liking' score 20 minutter efter dosering, hvilket faldt sammen med plasma Cmax. I modsætning hertil øgede den ækvivalente dosis d-amfetamin (50 mg intravenøst) ikke signifikant 'Dug liking' i forhold til placebo, og Cmax for plasma d-amfetamin forekom betydeligt senere ved 2,0 timer. Begge forbindelser gav ækvivalente AUC0-24h-værdier, men sammenlignet med den ækvivalente dosis IR d-amfetamin var Cmax for plasma d-amfetamin tre gange mindre for lisdexamfetamin, og tmax var tre gange større.
Førstehjælp i tilfælde af overdosering.
Toksicitetsmekanismen er primært relateret til overdreven ekstracellulær dopamin, noradrenalin og serotonin. Det primære kliniske syndrom involverer fremtrædende neurologiske og kardiovaskulære effekter, men sekundære komplikationer kan involvere nyre-, muskel-, lunge- og gastrointestinale effekter. Hyperaktivitet, hypertermi, takykardi, takypnø, mydriasis, tremor, kramper og ændret mental status er nogle af de mest almindelige tegn og symptomer på amfetaminforgiftning. Diagnosen kan bekræftes ved at påvise amfetamin i maveindhold eller opkast eller ved positiv urintoksikologi for ulovlige stoffer. Falsk positiv amfetaminscreening kan forekomme efter overdosering af trazodon eller bupropion. Der findes ingen modgift mod amfetamintoksicitet, men aktivt kul er en nødbehandling. Hos patienter, der kan drikke sikkert, anbefales det at give aktivt kul, 1 til 2 g/kg op til 100 g gennem munden, hvis indtagelsen er sket inden for den foregående time. Amfetaminrelateret toksicitet kræver håndtering ved at kontrollere livstruende tegn fra centralnervesystemet og hjerte-kar-systemet i et roligt miljø.
Indikationer for at tage på hospitalet eller tilkalde en ambulance: nedsat eller fraværende bevidsthed, nedsat tale, motorisk aktivitet, manglende orientering i rum og tid, stærke smerter bag brystbenet, der varer mere end en halv time, en stigning i kropstemperaturen på mere end 38,0 C eller hypertermi, der varer mere end en halv time, en stigning i blodtrykket på mere end 180/110 mmHg uden effekt af hypotensiv behandling.
1. Behandlingen af patienter med et blodtryk på mere end 140/95 mm Hg omfatter en tablet af en betablokker uden intrinsisk sympatomimetisk aktivitet, en tablet af en ACE-hæmmer, efter 30 minutter - en tablet af et beroligende middel (0,25 mg alprazolam).
2. Hos patienter med intens angst, panikanfald, psykose: en tablet af et beroligende middel og en tablet af et neuroleptikum med en beroligende effekt, psykologisk hjælp, akut psykoterapi.
3. Hos patienter med smerter i brystbenet, ubehag i brystet: en tablet af langsomme calciumkanalblokkere af tredje generation, reflektorisk reduktion af hjertefrekvensen, en tablet af en ACE-hæmmer af tredje generation ELLER en tablet af en agonist med imidazolineffekter ELLER en tablet ; hvis smertesyndromet ikke bliver mindre intenst inden for 20 minutter, anbefales det at tage på hospitalet.
4. Når der er en stigning i kropstemperaturen på højst 37,5 C, bestilles dynamisk observation i en halv time. Farmakologisk behandling er ikke nødvendig. Hvis hypertermi varer ved i mere end en halv time (i fravær af eksterne årsager), anbefales det at tage på hospitalet.
5. Hos patienter med intens hovedpine anbefales det at bruge antispasmodika i kombination med beroligende naturlægemidler eller beroligende midler i lave doser. Hvis hovedpinen er forbundet med opkastninger, anbefales en intramuskulær injektion af metoclopramid 2,0 ml. Isoleret kvalme og funktionel dyspepsi kræver ikke farmakologisk behandling.
6. Ved rystelser, moderate kramper eller mild psykomotorisk uro anbefales beroligende midler. Det frarådes på det kraftigste at bruge neuroleptika i disse tilfælde.
En betablokker som propranolol kan hjælpe med at håndtere takyarytmier i hjertet. Overvej intravenøs nitroprussid (start med 0,5 til 1 mcg/kg pr. minut og optitrer efter behov) ved svær hypertension. Intravenøs væske bør gives, da det modvirker hypertermi, hjælper med at opretholde nyrefunktionen og hjælper med at fremme elimineringen af amfetamin og dets analoger. I tilfælde af alvorlig agitation bør klinikere overveje aggressiv behandling for at undgå malign hypertension, rabdomyolyse, hypertermi og krampeanfald. Der er evidens for at bruge store doser benzodiazepiner til at behandle amfetamin-overdosis-relateret psykose og agitation. I tilfælde, hvor agitation, delirium og bevægelsesforstyrrelser ikke reagerer på benzodiazepiner, kan der gives andenvalgsbehandling med antipsykotika som ziprasidon eller haloperidol, centrale alfa-adrenoreceptoragonister som dexmedetomidin eller propofol. Neuromuskulær lammelse, intubation og aktiv nedkøling kan være nødvendigt i alvorlige tilfælde. Hos patienter med takykardi skal der tages EKG og overvejes telemetri. Brug intravenøs væske og sedation til at kontrollere hjertesymptomer. I tilfælde af svær hypertension bør man overveje intravenøs nitroprussid. Den bedste måde at håndtere rhabdomyolyse på er at starte med 0,9 % normalt saltvand og overvåge kreatinkinase (CK), elektrolytter og kreatinin.
Der er rapporter om Takotsubo-kardiomyopati (TTC), også kendt som stressinduceret kardiomyopati, som udløses af en overdosis amfetamin. I et tilfælde henvendte en patient sig på skadestuen efter at have indtaget 30 amfetaminsalttabletter med symptomer på brystsmerter og åndenød. På indlæggelsestidspunktet var hjerteenzymerne forhøjede, elektrokardiogrammet var ikke bemærkelsesværdigt, og ejektionsfraktionen (EF) var 25-30 % med svær hypokinesi. Men 24 timer senere var symptomerne forsvundet, og et gentaget ekkokardiogram udført tre dage senere viste en EF på 60 % uden regionale vægbevægelsesabnormiteter.
Regler for påvisning og opbevaring.
Som regel skal opbevaring af amfetaminracemat såvel som d-enantiomer ske på et sted, der er beskyttet mod lys og fugt, helst ved stuetemperatur eller ved en temperatur på mindst 5 C og højst 40 C. Det kan opbevares i madpapir eller i polyethylenterephthalatpakker uden metalindhold.
Efter en enkelt intranasal brug af dextroamfetamin er detektionsperioden i urinen ved brug af ekspresforskningsmetoder ca. 46-72 timer, med oral brug op til 120-220 timer. Langvarig systematisk brug af dextroamfetamin er ikke blevet undersøgt i forbindelse med identifikation af metabolitter, selvom det teoretisk er kendt, at der er stor chance for at påvise de vigtigste metabolitter ved PFIA eller kromatografi-massespektrometri i løbet af 1,5-2 måneder efter sidste brug af amfetamin (hvilket er mindre end for amfetaminracemat). Detektionsperioden for dextroamfetaminmetabolitter i hår er op til 2,5-3 måneder.
Syntese af dextroamfetamin fra P2P
Fysisk-kemiske egenskaber og former for stoffet.
Grundlæggende har dextroamfetamin såvel som amfetaminracemat udseendet af en farveløs flygtig olieagtig væske med en karakteristisk "fiskeagtig" lugt og er godt opløselig i organiske opløsningsmidler. Dens kogepunkt er 200-203 °C. Enantiomeren kan have et pulveragtigt udseende med dannelse af små "sten" i hvid eller lysegul/cremefarve, med en svag lugt, svagt hygroskopisk, delvist opløselig i vand, når den er i form af en tablet. Det findes oftest i form af sulfat, hydrochlorid, sucrat og meget sjældent i form af fosfat. Som regel er dextroamfetamin en del af forskellige lægemidler som "Aderral" og "Dexedrine", hvor det findes i form af sukrat og sulfat i koncentrationer på 25% af det samlede volumen. Det er også en del af "Vyvanse", "Elvanse", "Tyvense", hvor det er i den proaktive tilstand af dimesylat lysdexamfetamin; fermentering med l-lysin metaboliserer det til den aktive form af d-amfetamin; "Dexedrine". Andre handelsnavne på lægemidler omfatter: Dexedrinsulfat, Afatin, d-Amfetasul, Domafate Obesedrin, Dexten, Maxiton, Sympamin, Simpamina-D, Albemap, Dadex, Ardex, Dexalone, Amsustain, Betafedrina, d-Betaphedrin, Diocurb, Dextrostat.
Farmakokinetik.
Når det indgives, metaboliseres amfetamin ved hydroxylering, hvor det vigtigste cytokrom er CYP2D6, beta-hydroxylering (DBH) og oxidativ deaminering (FMO3); der er andre enzymer, der er mindre involveret i metaboliseringen af amfetamin, såsom butyrat-CoA-ligase og glycin-N-acyltransferase. Biotilgængeligheden (med uændret gastrointestinal pH) når 70-75% for racemat og op til 80-83% for dextroamfetamin. Bindingen med plasmaproteiner når 15-30% ifølge forskellige kilder hos raske mennesker, distributionsvolumenet er moderat, stoffet passerer aktivt gennem blod-hjerne-barrieren med en variabel koefficient på 17p. T1/2 er ca. 7-15 timer, afhængigt af mange faktorer, herunder urinens pH (med en acceleration af halveringstiden ved lavere værdier). Imax - 15-70 minutter. Dødelig dosis af d-isomer af amfetamin er ikke blevet undersøgt; der er dog teoretiske konklusioner om store værdier af LD 50 på 5-10% fra de tilgængelige ekstrapolerede data for standardracematet af amfetaminsulfat (98-130 mg/kg). Amfetamin elimineres i næsten de samme kvalitative indikatorer for kendte metabolitter, men mængden af hippursyre, benzoylglycuronid og norephedrin er betydeligt mindre (60 % af de samlede data), hvilket skyldes dette racemats specificitet i forbindelse med metabolisme på deamineringsniveau. I undersøgelser af gnavere blev der påvist et markant fald i genotoksicitet i modsætning til standardamfetaminracematet i en dosis på 4600 mg/ml.
Virkningsmekanisme.
Den farmakodynamiske virkningsmekanisme adskiller sig næsten ikke fra den grundlæggende form af amfetamin. Gennem hæmning og reversering af serotonin-, noradrenalin- og dopamintransportører, interaktion med TAAR1, hvilket i sidste ende fører til en stigning i koncentrationen af monoaminer og katekolaminer samtidigt i den synaptiske kløft (kløften er 10-50 nm bred mellem membranerne, kanterne styrkes af intercellulære kontakter). Et vigtigt træk ved dextroamfetamin specifikt er det faktum, at affiniteten for den højresidede enantiomer med TAAR1 er meget større (med 15-30% ifølge forskellige kilder), og VMAT2 fanger en mindre mængde af denne enantiomer, og den mindste affinitet for serotonintransportøren i modsætning til den venstresidede, og belastningen af sådanne systemer som CDK5R1, DLG1 og CAMKIIAA er betydeligt mindre med tilsvarende kliniske virkninger.
Ikke mindre vigtigt er det videnskabelige faktum identificeret af Novascreen BioSciences Corporation, at på grund af lavere affinitet for en række receptorer (a1, a2, b-adrenoreceptorer, mu-opioid, histamin, CCK, NK, GABA, ETeA og andre) er sværhedsgraden af både uønskede kliniske bivirkninger og andre negative konsekvenser på molekylært niveau betydeligt lavere, hvilket bestemmer prioriteringen af denne særlige form for stoffet med bevarelse af de tilsvarende ønskede kliniske virkninger. Nettoeffekten af disse multiple virkningsegenskaber er, at d-amfetamin øger "tilgængeligheden" eller koncentrationsevnen af katekolaminer i det ekstracellulære rum ved at vende transporten af katekolaminer fra den terminale ende af neuronet, hvilket også er et af kendetegnene ved den højredrejende enantiomer. Indikatorerne for hæmning af optagelsen af [3 H] i rottehjernens synaptosomer af d-enantiomeren varierer og adskiller sig markant fra amfetaminracemat. For noradrenalin er Ki = nM ved en værdi på 45-50, for dopamin 82-200, for 5-HT varierer indikatorerne fra 1840 til 3830 i rottehjernemodeller. En mere "blød" effekt af afhængighedscyklussen fra denne form for amfetamin er en konsekvens af en relativt lavere overekspression af FosB i nucleus accumbens, tilstedeværelsen af positive effekter og fraværet af inhibering af CREB af protein- og serinfosfotaser netop på grund af lavere affinitet og indflydelse på de glutamaterge og serotoninerge systemer. Neurokemiske virkninger har til sammenligning også en særlig evne; i Heal- og Wickens-undersøgelserne blev der påvist ændringer i motorisk aktivitet, hvor dens maksimale værdi var 3-4 gange mindre end ved indtagelse af amfetaminhydrochlorid eller sulfat, hvilket er direkte relateret til hastigheden og den molekylære korrektion af dopaminudstrømningen i hjernens striatum.
Selvom in vitro-eksperimenter giver et godt indblik i individuelle mekanismer, kan effekten af amfetamin i forhold til andre indirekte monoaminagonister, for eksempel klassiske genoptagelseshæmmere, kun estimeres ud fra in vivo-eksperimenter. Vi har brugt intracerebral mikrodialyse med to sonder til at undersøge in vivo-effekterne af d- og l-amfetamin i den spontant hypertensive rotte (SHR), som er blevet foreslået som en gnavermodel for ADHD. Begge isomerer af amfetamin øgede dosisafhængigt de ekstracellulære koncentrationer af noradrenalin i den præfrontale cortex (PFC) og dopamin i striatum. Farmakodynamikken i deres virkninger er typisk for dem, der er rapporteret for monoaminfrigørende midler, dvs. en hurtig virkning med maksimale stigninger i noradrenalin- og dopaminudstrømning, der forekommer efter 30-45 minutter, store virkninger (400-450 % af baseline for noradrenalin og 700-1500 % af baseline for dopamin) med et relativt hurtigt fald efter maksimum. Selvom der ikke er medtaget nogen sammenlignende resultater i denne gennemgang, er omfanget af de stigninger, der produceres af amfetamins isomerer, større end dem, der er rapporteret for klassiske genoptagelseshæmmere som atomoxetin eller bupropion, og der er ikke noget dosis-effekt-loft for amfetamins handlinger.
Når man sammenligner stoffernes virkning på udstrømningen af katekolaminer i PFC, er det vigtigt at tage højde for den meget usædvanlige neuroanatomi i dette hjerneområde. Tætheden af DAT-steder på dopaminerge neuroner i PFC er meget lav, og som følge heraf bliver det meste dopamin, der frigives, bundet via NET i noradrenerge neuroner. Selv om der er få DAT-steder på dopaminerge neuroner i PFC, er deres genoptagelseskapacitet tilstrækkelig til, at amfetamin kan fremkalde en betydelig dopaminfrigivelse fra dem, selv om det er blevet foreslået, at en stor del af dopaminfrigivelsen i PFC kommer fra noradrenerge neuroner. I Shires udviklingsstudier på in vivo-modeller blev der påvist en statistisk signifikant forskel. D-AMP påvirkede de kognitive komponenter i impulskontrol forskelligt: andelen af impulsive valg faldt med samme niveau af belønning, hvilket også bekræfter effektiviteten af denne enantiomer.
Anvendelsesmetoder og doser.
Rekreativ dosering af amfetamin d-enantiomer starter fra 40-60 mg ved oral brug, i tilfælde af nuværende tolerance kan startdosis øges op til 120-160 mg ved en enkelt oral brug. Ved intranasal administration anbefales det at bruge en startdosis på 30-50 mg. Parenteral administration af denne form er kun tilladt i tilfælde af, at der opnås en ren opløsning. Eventuelle tabletter eller pulvere anbefales kun til brug ved oral og intranasal administration. Ved parenteral indgivelse er startdosis 0,15-0,24 mg/kg.
Klinisk præsentation af amfetaminforgiftning.
Symptomerne ovenfor er "milde", deres sværhedsgrad er op til 40% mindre end for den kombinerede form. Derfor forekommer sådanne negative uønskede virkninger som vandladningsbesvær, hjerterytmeforstyrrelser, øget hjertefrekvens, øget blodtryk, øget svedtendens, høj kropstemperatur, kvalme, pupiludvidelse udelukkende ved høje doser og er proportionalt forskellige i sammenligning med racemat.
1. Eufori og en følelse af øget energi;
2. Langvarig vågenhed;
3. Grandiose ideer eller handlinger;
4. Voldelig eller aggressiv adfærd;
5. Bekræftelsesbias;
6. Labilitet i humøret;
7. Adfærd præget af gentagne stereotyper;
8. Auditive, visuelle eller taktile illusioner;
9. Forvrængning af personlighed;
10. Undertrykkelse af appetitten.
Personer, der bruger D-AMP, skal også have mindst to af følgende tegn for at blive diagnosticeret:
1. Takykardi;
2. Arteriel hypertension;
3. Sved og feberagtige kulderystelser;
4. Kvalme eller opkastning;
5. Muskelsvaghed;
6. Smerter eller ubehag bag brystbenet;
7. Psykomotorisk uro;
8. Udvidelse af pupiller.
Symptomer på D-AMP-forgiftning omfatter hovedsageligt tegn på komplikationer i hjerte-kar-systemet og nervesystemet. Åndedrætsforstyrrelser udvikles sjældnere.
Hjerteforstyrrelser: hypertension og takykardi er de mest almindelige, når man tager lave doser. Indledende bradykardi er også mulig på grund af en stigning i den parasympatiske tone. Arytmier (supraventrikulære er hyppige) kan være forårsaget af en sympatisk krise eller en blokade af hurtige natriumkanaler. Iskæmi og myokardieinfarkt forårsages af koronar spasme, som når et maksimum 30 minutter efter intranasal D-AMP-brug og falder sammen med den højeste koncentration af stoffet i blodet. Yderligere koronarspasmer kan udvikles efter 90 minutter, hvilket er forbundet med ophobning af D-AMP-metabolitter. En stigning i blodpladeaggregering fører til dannelse af blodpropper i koronarkarrene. Desuden øges myokardiets iltbehov. En sjælden komplikation er aortaruptur.
Særlige instruktioner, interaktioner med andre stoffer.
De absolutte kontraindikationer for brugen af enhver form for amfetamin er: alvorlig vaskulær aterosklerose, enhver symptomatisk kardiovaskulær sygdom, MAO-indtagelse (og 14 dage efter den sidste brug af stoffet i denne gruppe), glaukom, hyperthyreoidisme.
"Ikke-ADIOS"-reglen:
Non-Alcohol - det anbefales ikke at bruge sammen med alkohol.
Non-Dissociatives - det anbefales ikke at bruge sammen med dissociative stoffer.
Non-iMAO - det anbefales ikke at bruge det sammen med monoaminoxidasehæmmere.
Non-Opiates - det anbefales ikke at bruge sammen med opioidreceptoragonister.
Ikke-stimulatorer - det anbefales ikke at bruge sammen med stimulanser.
1. Når man bruger D-AMP sammen med lægemidler fra gruppen af PDE-5-hæmmere, øges risikoen for at udvikle bivirkninger af begge stoffer. Mest almindelige bivirkninger: svær hovedpine af spastisk karakter, kvalme. Forekomsten af alvorlige kritiske tilstande er lav.
2. Ved brug af D-AMP sammen med marihuana er der risiko for forekomst af forhøjet blodtryk, hovedpine, fin tremor, tørhed i munden. Sandsynligheden for at udvikle alvorlige kritiske tilstande er lav.
3. Ved brug af D-AMP sammen med neuroleptika/tranquilizers er der stor risiko for at udjævne D-AMP's hovedvirkninger. Sandsynligheden for at udvikle alvorlige kritiske tilstande er lav (i tilfælde, hvor der ikke er kontraindikationer for at tage neuroleptika).
4. Det anbefales ikke at bruge D-AMP under behandling med antibakterielle, antivirale og svampedræbende lægemidler, hormoner og antikoagulantia.
5. Det anbefales ikke at bruge D-AMP under kirurgiske indgreb og i tiden før og efter det i en bestemt periode (perioden identificeres individuelt).
6. Det anbefales ikke at bruge D-AMP, hvis der er diagnosticeret en lidelse i det kardiovaskulære system, nyrerne, leveren, lungerne eller centralnervesystemet.
7. Det anbefales ikke at bruge D-AMP under graviditet og amning.
I to tidligere offentliggjorte undersøgelser sammenlignede Jasinski og Krishnan de subjektive virkninger af IR d-amfetamin hos stoferfarne frivillige mennesker, når disse forbindelser blev administreret intravenøst og oralt. I forsøget, hvor de sammenlignede disse stoffer efter oral administration, fremkaldte IR d-amfetamin (40 mg (29,6 mg d-amfetaminbase)) en statistisk signifikant stigning i forhold til placebo i "Drug liking" på Drug Rating Questionnaire - Subject (DQRS)-skalaen, hvorimod den tilsvarende dosis d-amfetamin (100 mg, oral) ikke gjorde det. Desuden var tidspunktet for den maksimale farmakologiske virkning af d-amfetamin væsentligt forsinket sammenlignet med IR d-amfetamin, nemlig 3,0 timer mod 1,5-2,0 timer. Når d-amfetamin blev givet i en øget dosis på 150 mg, øgede det signifikant DQRS-scoren for "Drug liking" i samme omfang som IR d-amfetamin (40 mg oralt). Imidlertid var den maksimale effekt af den højere dosis d-amfetamin endnu mere forsinket, ved 4.0 h. Når den intravenøse rute blev udforsket, producerede IR d-amfetamin (20 mg intravenøs) en maksimal 'Drug liking' score 20 minutter efter dosering, hvilket faldt sammen med plasma Cmax. I modsætning hertil øgede den ækvivalente dosis d-amfetamin (50 mg intravenøst) ikke signifikant 'Dug liking' i forhold til placebo, og Cmax for plasma d-amfetamin forekom betydeligt senere ved 2,0 timer. Begge forbindelser gav ækvivalente AUC0-24h-værdier, men sammenlignet med den ækvivalente dosis IR d-amfetamin var Cmax for plasma d-amfetamin tre gange mindre for lisdexamfetamin, og tmax var tre gange større.
Førstehjælp i tilfælde af overdosering.
Toksicitetsmekanismen er primært relateret til overdreven ekstracellulær dopamin, noradrenalin og serotonin. Det primære kliniske syndrom involverer fremtrædende neurologiske og kardiovaskulære effekter, men sekundære komplikationer kan involvere nyre-, muskel-, lunge- og gastrointestinale effekter. Hyperaktivitet, hypertermi, takykardi, takypnø, mydriasis, tremor, kramper og ændret mental status er nogle af de mest almindelige tegn og symptomer på amfetaminforgiftning. Diagnosen kan bekræftes ved at påvise amfetamin i maveindhold eller opkast eller ved positiv urintoksikologi for ulovlige stoffer. Falsk positiv amfetaminscreening kan forekomme efter overdosering af trazodon eller bupropion. Der findes ingen modgift mod amfetamintoksicitet, men aktivt kul er en nødbehandling. Hos patienter, der kan drikke sikkert, anbefales det at give aktivt kul, 1 til 2 g/kg op til 100 g gennem munden, hvis indtagelsen er sket inden for den foregående time. Amfetaminrelateret toksicitet kræver håndtering ved at kontrollere livstruende tegn fra centralnervesystemet og hjerte-kar-systemet i et roligt miljø.
Indikationer for at tage på hospitalet eller tilkalde en ambulance: nedsat eller fraværende bevidsthed, nedsat tale, motorisk aktivitet, manglende orientering i rum og tid, stærke smerter bag brystbenet, der varer mere end en halv time, en stigning i kropstemperaturen på mere end 38,0 C eller hypertermi, der varer mere end en halv time, en stigning i blodtrykket på mere end 180/110 mmHg uden effekt af hypotensiv behandling.
1. Behandlingen af patienter med et blodtryk på mere end 140/95 mm Hg omfatter en tablet af en betablokker uden intrinsisk sympatomimetisk aktivitet, en tablet af en ACE-hæmmer, efter 30 minutter - en tablet af et beroligende middel (0,25 mg alprazolam).
2. Hos patienter med intens angst, panikanfald, psykose: en tablet af et beroligende middel og en tablet af et neuroleptikum med en beroligende effekt, psykologisk hjælp, akut psykoterapi.
3. Hos patienter med smerter i brystbenet, ubehag i brystet: en tablet af langsomme calciumkanalblokkere af tredje generation, reflektorisk reduktion af hjertefrekvensen, en tablet af en ACE-hæmmer af tredje generation ELLER en tablet af en agonist med imidazolineffekter ELLER en tablet ; hvis smertesyndromet ikke bliver mindre intenst inden for 20 minutter, anbefales det at tage på hospitalet.
4. Når der er en stigning i kropstemperaturen på højst 37,5 C, bestilles dynamisk observation i en halv time. Farmakologisk behandling er ikke nødvendig. Hvis hypertermi varer ved i mere end en halv time (i fravær af eksterne årsager), anbefales det at tage på hospitalet.
5. Hos patienter med intens hovedpine anbefales det at bruge antispasmodika i kombination med beroligende naturlægemidler eller beroligende midler i lave doser. Hvis hovedpinen er forbundet med opkastninger, anbefales en intramuskulær injektion af metoclopramid 2,0 ml. Isoleret kvalme og funktionel dyspepsi kræver ikke farmakologisk behandling.
6. Ved rystelser, moderate kramper eller mild psykomotorisk uro anbefales beroligende midler. Det frarådes på det kraftigste at bruge neuroleptika i disse tilfælde.
En betablokker som propranolol kan hjælpe med at håndtere takyarytmier i hjertet. Overvej intravenøs nitroprussid (start med 0,5 til 1 mcg/kg pr. minut og optitrer efter behov) ved svær hypertension. Intravenøs væske bør gives, da det modvirker hypertermi, hjælper med at opretholde nyrefunktionen og hjælper med at fremme elimineringen af amfetamin og dets analoger. I tilfælde af alvorlig agitation bør klinikere overveje aggressiv behandling for at undgå malign hypertension, rabdomyolyse, hypertermi og krampeanfald. Der er evidens for at bruge store doser benzodiazepiner til at behandle amfetamin-overdosis-relateret psykose og agitation. I tilfælde, hvor agitation, delirium og bevægelsesforstyrrelser ikke reagerer på benzodiazepiner, kan der gives andenvalgsbehandling med antipsykotika som ziprasidon eller haloperidol, centrale alfa-adrenoreceptoragonister som dexmedetomidin eller propofol. Neuromuskulær lammelse, intubation og aktiv nedkøling kan være nødvendigt i alvorlige tilfælde. Hos patienter med takykardi skal der tages EKG og overvejes telemetri. Brug intravenøs væske og sedation til at kontrollere hjertesymptomer. I tilfælde af svær hypertension bør man overveje intravenøs nitroprussid. Den bedste måde at håndtere rhabdomyolyse på er at starte med 0,9 % normalt saltvand og overvåge kreatinkinase (CK), elektrolytter og kreatinin.
Der er rapporter om Takotsubo-kardiomyopati (TTC), også kendt som stressinduceret kardiomyopati, som udløses af en overdosis amfetamin. I et tilfælde henvendte en patient sig på skadestuen efter at have indtaget 30 amfetaminsalttabletter med symptomer på brystsmerter og åndenød. På indlæggelsestidspunktet var hjerteenzymerne forhøjede, elektrokardiogrammet var ikke bemærkelsesværdigt, og ejektionsfraktionen (EF) var 25-30 % med svær hypokinesi. Men 24 timer senere var symptomerne forsvundet, og et gentaget ekkokardiogram udført tre dage senere viste en EF på 60 % uden regionale vægbevægelsesabnormiteter.
Regler for påvisning og opbevaring.
Som regel skal opbevaring af amfetaminracemat såvel som d-enantiomer ske på et sted, der er beskyttet mod lys og fugt, helst ved stuetemperatur eller ved en temperatur på mindst 5 C og højst 40 C. Det kan opbevares i madpapir eller i polyethylenterephthalatpakker uden metalindhold.
Efter en enkelt intranasal brug af dextroamfetamin er detektionsperioden i urinen ved brug af ekspresforskningsmetoder ca. 46-72 timer, med oral brug op til 120-220 timer. Langvarig systematisk brug af dextroamfetamin er ikke blevet undersøgt i forbindelse med identifikation af metabolitter, selvom det teoretisk er kendt, at der er stor chance for at påvise de vigtigste metabolitter ved PFIA eller kromatografi-massespektrometri i løbet af 1,5-2 måneder efter sidste brug af amfetamin (hvilket er mindre end for amfetaminracemat). Detektionsperioden for dextroamfetaminmetabolitter i hår er op til 2,5-3 måneder.
Last edited:
